近年来,发展选择性合成含有连续手性中心化合物的所有立体异构体的方法成为不对称合成中一个重要的研究目标,同时也是一个极具挑战性的研究方向。在这一领域中,使用铱催化的不对称烯丙基取代反应体系与其催化体系相结合的双催化策略取得了重要进展。Carreira、Jørgensen、Hartwig、张万斌和王春江等课题做出了非常优秀的工作。值得注意的是,在这些反应中都需要使用两种不同的手性催化剂,通过不同绝对构型的催化剂之间的组合实现目标分子所有立体异构体的选择性合成(图1a)。
含氟手性化合物存在于很多医药和农药分子中。尽管目前已有许多合成含氟手性化合物的方法,然而构建含氟季碳手性中心的方法仍十分有限。其中,构建包含连续手性中心(其中一个为链接碳氟键的季碳中心)的分子极具挑战性。因此发展该类化合物的合成方法,特别是发展能实现对这类化合物的立体发散性合成的方法具有重要意义。
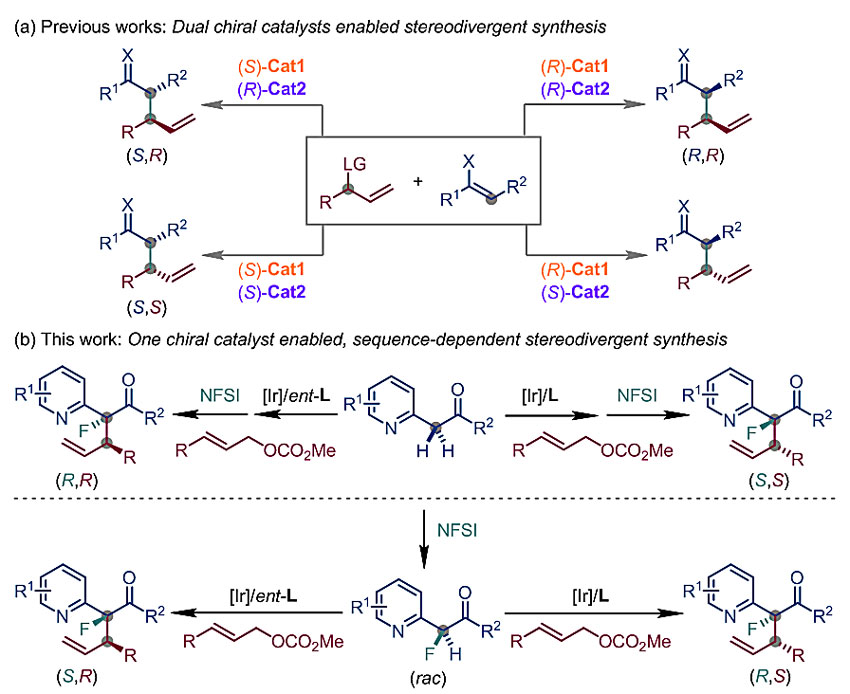
图1. 不对称催化立体发散性合成策略
最近,中国科学院上海有机化学所游书力研究员(点击查看介绍)团队发展了一种新颖的策略实现了α-吡啶-α-氟代酮类化合物的立体发散性合成(图1b)。产物分子中含有两个连续手性中心,其中一个为链接碳氟键的季碳中心。该策略以α-吡啶酮类化为起始原料,仅通过调控铱催化不对称烯丙基取代反应和亲电氟化反应的顺序及变换铱不对称烯丙基取代反应中配体的绝对构型,能够实现对目标产物的四种立体异构体的合成。与文献报道的不对称催化立体发散性合成策略使用两个手性催化剂相比,本工作仅使用了一个手性催化剂,为实现含两个(或多个)手性中心化合物的所有立体异构体的合成提供了新的研究思路。
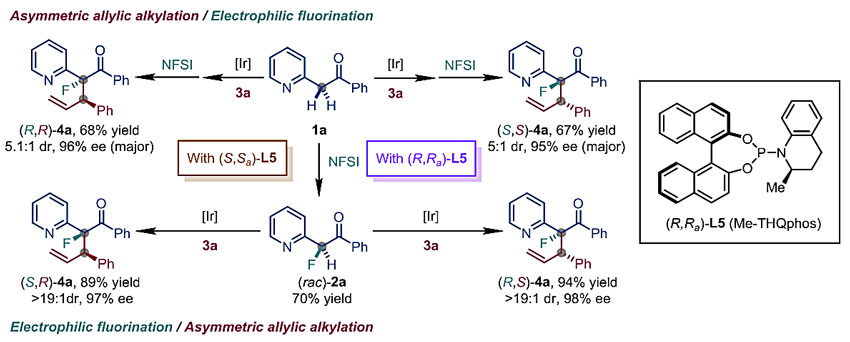
图2. 立体发散性合成手性α-吡啶-α-氟代酮类化合物
该工作的部分结果近期发表于Angew. Chem. Int. Ed.,第一作者为刘喜佳博士。该工作得到科技部、国家自然科学基金委、中国科学院和上海有机化学研究所的大力支持。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Sequence-Dependent Stereodivergent Allylic Alkylation/Fluorination Reaction of Acyclic Ketones
Xi-Jia Liu, Shicheng Jin, Wen-Yun Zhang, Qiang-Qiang Liu, Chao Zheng, Shuli You
Angew. Chem. Int. Ed., 2019, DOI: 10.1002/anie.201912882
导师介绍
游书力
https://www.x-mol.com/university/faculty/15598
(本稿件来自Wiley)
 0
0










